Đốt cháy hoàn toàn 3,74 gam hỗn hợp X gồm CH3COOH; CH3COOCxHy; CxHyOH thu được 3,584 lít CO2 (đktc) và 3,42 gam H2O. Mặt khác, cho 3,74 gam X phản ứng hết với 40ml dung dịch NaOH 1M, thu được dung dịch Y và 0,05 mol CxHyOH. Cô cạn dung dịch Y, thu được 2,86 gam chất rắn khan. Trả lời câu hỏi dưới đây:Xác định công thức phân tử của ancol CxHyOH?

Câu hỏi
Nhận biếtĐốt cháy hoàn toàn 3,74 gam hỗn hợp X gồm CH3COOH; CH3COOCxHy; CxHyOH thu được 3,584 lít CO2 (đktc) và 3,42 gam H2O. Mặt khác, cho 3,74 gam X phản ứng hết với 40ml dung dịch NaOH 1M, thu được dung dịch Y và 0,05 mol CxHyOH. Cô cạn dung dịch Y, thu được 2,86 gam chất rắn khan.
Trả lời câu hỏi dưới đây:
Xác định công thức phân tử của ancol CxHyOH?
Đáp án đúng: B
Lời giải của Luyện Tập 365
CTPT của ancol:
Ta có sơ đồ cháy X: X + O2 → CO2 + H2O
Số mol CO2 = 3,584 : 22,4 = 0,16 mol
Số mol H2O = 3,42 : 18 = 0,19 mol
Từ các PTHH của phản ứng chảy:
Ta có: CH3COOH và este CH3COOCxHy trong đó gốc CxHy hóa trị 1 và no, khi cháy tạo thành số mol H2O bằng số mol CO2.
Theo đề ra:
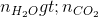 =>CxHyOH là ancol no đơn chức: y = 2x+1
=>CxHyOH là ancol no đơn chức: y = 2x+1
Từ đó ta có: 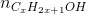 = 0,19 - 0,16 = 0,03 mol
= 0,19 - 0,16 = 0,03 mol
Sau khi thủy phân thu được tổng số mol ancol là 0,05 mol
Suy ra: số mol este CH3COOCxH2x+1 là: 0,05 – 0,03 = 0,02 mol
Vậy X gồm: CH3COOH (a mol); CH3COOCxH2x+1 (0,02 mol)
Và CxH2x+1OH (0,03 mol)
PTHH của phản ứng với dung dịch NaOH của X:
CH3COOH + NaOH → CH3COONa + H2O
a → a → a (mol)
CH3COOCxHy + NaOH → CH3COONa + CxHyOH
0,02→ 0,02→ 0,02→ 0,02
- Nếu NaOH phản ứng vừa đủ với X, chất rắn là CH3COONa
Số mol CH3COONa = nNaOH = 0,04 mol => Khối lượng CH3COONa = 0,04 . 82 = 3,28 gam > 2,86 gam
- Vậy NaOH còn dư
Ta có: mrắn khan = 82.(0,02+a) + 40.[0,04 –(0,02 +a)] = 2,86 gam => a= 0,01
=>mX = 0,01 . 60 + 0,02(60+14n)+ 0,03.(14n+18) = 3,74 => n=2
=>CTPT của ancol là C2H5OH
CTPT của ancol:
Ta có sơ đồ cháy X: X + O2 → CO2 + H2O
Số mol CO2 = 3,584 : 22,4 = 0,16 mol
Số mol H2O = 3,42 : 18 = 0,19 mol
Từ các PTHH của phản ứng chảy:
Ta có: CH3COOH và este CH3COOCxHy trong đó gốc CxHy hóa trị 1 và no, khi cháy tạo thành số mol H2O bằng số mol CO2.
Theo đề ra:
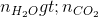 =>CxHyOH là ancol no đơn chức: y = 2x+1
=>CxHyOH là ancol no đơn chức: y = 2x+1
Từ đó ta có: 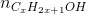 = 0,19 - 0,16 = 0,03 mol
= 0,19 - 0,16 = 0,03 mol
Sau khi thủy phân thu được tổng số mol ancol là 0,05 mol
Suy ra: số mol este CH3COOCxH2x+1 là: 0,05 – 0,03 = 0,02 mol
Vậy X gồm: CH3COOH (a mol); CH3COOCxH2x+1 (0,02 mol)
Và CxH2x+1OH (0,03 mol)
PTHH của phản ứng với dung dịch NaOH của X:
CH3COOH + NaOH → CH3COONa + H2O
a → a → a (mol)
CH3COOCxHy + NaOH → CH3COONa + CxHyOH
0,02→ 0,02→ 0,02→ 0,02
- Nếu NaOH phản ứng vừa đủ với X, chất rắn là CH3COONa
Số mol CH3COONa = nNaOH = 0,04 mol => Khối lượng CH3COONa = 0,04 . 82 = 3,28 gam > 2,86 gam
- Vậy NaOH còn dư
Ta có: mrắn khan = 82.(0,02+a) + 40.[0,04 –(0,02 +a)] = 2,86 gam => a= 0,01
=>mX = 0,01 . 60 + 0,02(60+14n)+ 0,03.(14n+18) = 3,74 => n=2
=>CTPT của ancol là C2H5OH
Câu hỏi liên quan
-

Cho sơ đồ chuyển hóa sau:
Hãy xác định các chất A, B, C, D, E, F, G, H. Viết các phương trình phản ứng hóa học xảy ra (ghi rõ điều kiện nếu có). Biết rằng:
- A, B, C, D là các hợp chất hữu cơ; E, F, G, H là các hợp chất vô cơ
- A tác dụng với dung dịch iot thấy xuất hiện màu xanh
- E tác dụng với H tạo ra F; F không tác dụng được với H
- G tác dụng được với dung dịch AgNO3 tạo kết tủa màu trắng
-

Lấy một thanh sắt nặng 16,8 gam cho vào 2 lít dung dịch hỗn hợp AgNO3 0,2M và Cu(NO3)2 0,1M. Thanh sắt có tan hết không? Tính nồng độ mol của chất tan có trong dung dịch thu được sau phản ứng. Biết các phản ứng xảy ra hoàn toàn và thể tích dung dịch thay đổi không đáng kể
-

Cho từ từ dung dịch NaOH 2M vào dung dịch Y và khuấy đều đến khi thấy bắt đầu xuất hiện kết tủa thì dùng hết V1 lít dung dịch NaOH 2M, tiếp tục cho tiếp dung dịch NaOH vào đến khi lượng kết tủa không có sự thay đổi nữa thì lượng dung dịch NaOH 2M đã dùng hết 600ml. Tìm các giá trị m và V1
-

Hòa tan hoàn toàn 0,297 gam hỗn hợp Natri và một kim loại thuộc nhóm IIA trong bảng tuần hoàn các nguyên tố hóa học vào nước. Ta được dung dịch X và 56ml khí Y (đktc). Xác định kim loại thuộc nhóm IIA và khối lượng của mỗi kim loại trong hỗn hợp
-

Hiđrocacbon X là chất khí (ở nhiệt độ phòng, 250C). Nhiệt phân hoàn toàn X (trong điều kiện không có oxi) thu được sản phẩm C và H2, trong đó thể tích khí H2 thu được gấp đôi thể tích khí X (đo ở cùng điều kiện). Xác định các công thức phân tử thỏa mãn X
-

Hỗn hợp X gồm ba kim loại Al, Fe, Cu.
Cho m gam hỗn hợp X vào dung dịch CuSO4 (dư) sau khi phản ứng xảy ra hoàn toàn thu được 35,2 gam kim loại. Nếu cũng hòa tan m gam hỗn hợp X vào 500ml dung dịch HCl 2M đến khi phản ứng xảy ra hoàn toàn thu được 8,96 lít khí H2 (đktc), dung dịch Y và a gam chất rắn
Trả lời câu hỏi dưới đây:
-

Tìm công thức phân tử, công thức cấu tạo của A, A1, C, B
-

Hỗn hợp khí X gồm hai hiđrocacbon A và B (MA < MB) có thể tích bằng nhau. Đốt cháy hoàn toàn 1 lít X trong khí O2 thu được 1,5 lít khí CO2 và 1,5 lít hơi nước. Xác định công thức phân tử của các hiđrocacbon A và B. Biết rằng thể tích của các khí và hơi nước đo ở cùng điều kiện nhiệt độ và áp suất
-

Một hỗn hợp gồm Al, Fe, Cu và Ag. Bằng phương pháp hóa học hãy tách rời hoàn toàn các kim loại ra khỏi hỗn hợp trên và cho biết các hóa chất cần sử dụng là gì?
-

Trộn V1 lít dung dịch H2SO4 0,3M với V2 lít dung dịch NaOH 0,4M thu được 0,6 lít dung dịch A. Tính V1, V2. Biết rằng 0,6 lít dung dịch A hòa tan vừa đủ 0,54 gam Al và các phản ứng xảy ra hoàn toàn
