X và Y là các dung dịch HCl có nồng độ khác nhau. Lấy V1 lít X trộn với V2 lít Y được 2 lít dung dịch Z (cho rằng sự pha trộn không làm thay đổi thể tích của dung dịch). Trả lời câu hỏi dưới đây:Tính nồng độ mol của các dung dịch X và Y, biết rằng nếu cho 0,1 lít X phản ứng hết với Fe thì lượng hidro thoát ra nhiều hơn so với 0,1 lít Y phản ứng hết với Fe là 448 ml (đktc).

Câu hỏi
Nhận biếtX và Y là các dung dịch HCl có nồng độ khác nhau. Lấy V1 lít X trộn với V2 lít Y được 2 lít dung dịch Z (cho rằng sự pha trộn không làm thay đổi thể tích của dung dịch).
Trả lời câu hỏi dưới đây:
Tính nồng độ mol của các dung dịch X và Y, biết rằng nếu cho 0,1 lít X phản ứng hết với Fe thì lượng hidro thoát ra nhiều hơn so với 0,1 lít Y phản ứng hết với Fe là 448 ml (đktc).
Đáp án đúng: D
Lời giải của Luyện Tập 365
Số mol H2 = 0,448 : 22,4 = 0,02 mol
PTHH:
2HCl + Fe → FeCl2 + H2
Gọi nồng độ mol của dung dịch HCl trong dung dịch X là CX
Nồng độ mol của HCl trong dung dịch Y là Cy
=>nHCl trong 0,1 lít dd X = 0,1CX ; nHCl trong 0,1 lít dd Y = 0,1CY
Khi 0,1 lít dung dịch X phản ứng với Fe =>số mol H2 =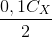
Khi 0,1 lít dd Y phản ứng với Fe => số mol H2 = 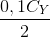
Theo đề ra: 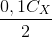 -
- 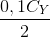 = 0,02
= 0,02
=>Cx = 0,4 + CY (*)
Mặt khác ta có: V1 lít X trộn với V2 lít Y được 2 lít dung dịch Z (sự pha trộn không làm thay đổi thể tích của dung dịch).
Vậy V1 + V2 = 2
=>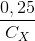 +
+ 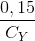 = 2
= 2
=>0,15CX + 0,25CY = 2CXCY (**)
Từ (*) và (**)
=>2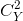 + 0,4Cy – 0,06 = 0
+ 0,4Cy – 0,06 = 0
Giải phương trình bậc hai: CY = 0,1 M
=>CX = 0,4 + 0,1 = 0,5 M
Số mol H2 = 0,448 : 22,4 = 0,02 mol
PTHH:
2HCl + Fe → FeCl2 + H2
Gọi nồng độ mol của dung dịch HCl trong dung dịch X là CX
Nồng độ mol của HCl trong dung dịch Y là Cy
=>nHCl trong 0,1 lít dd X = 0,1CX ; nHCl trong 0,1 lít dd Y = 0,1CY
Khi 0,1 lít dung dịch X phản ứng với Fe =>số mol H2 =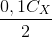
Khi 0,1 lít dd Y phản ứng với Fe => số mol H2 = 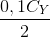
Theo đề ra: 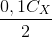 -
- 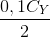 = 0,02
= 0,02
=>Cx = 0,4 + CY (*)
Mặt khác ta có: V1 lít X trộn với V2 lít Y được 2 lít dung dịch Z (sự pha trộn không làm thay đổi thể tích của dung dịch).
Vậy V1 + V2 = 2
=>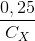 +
+ 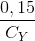 = 2
= 2
=>0,15CX + 0,25CY = 2CXCY (**)
Từ (*) và (**)
=>2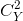 + 0,4Cy – 0,06 = 0
+ 0,4Cy – 0,06 = 0
Giải phương trình bậc hai: CY = 0,1 M
=>CX = 0,4 + 0,1 = 0,5 M
Câu hỏi liên quan
-

Cho hỗn hợp A gồm các chất (K2O, Ca(NO3)2, NH4NO3, KHCO3) có số mol bằng nhau vào nước (dư), sau khi các phản ứng xảy ra hoàn toàn, đun nóng đến khi không còn khí thoát ra, thu được dung dịch B. Xác định chất tan và môi trường của dung dịch B
-

Chỉ dùng thêm thuốc thử duy nhất là dung dịch KOH, thứ tự nhận biết các dung dịch và nêu phương pháp phân biệt các dung dịch sau: Na2CO3, MgSO4, CH3COOH, C2H5OH
-

Cho từ từ dung dịch NaOH 2M vào dung dịch Y và khuấy đều đến khi thấy bắt đầu xuất hiện kết tủa thì dùng hết V1 lít dung dịch NaOH 2M, tiếp tục cho tiếp dung dịch NaOH vào đến khi lượng kết tủa không có sự thay đổi nữa thì lượng dung dịch NaOH 2M đã dùng hết 600ml. Tìm các giá trị m và V1
-

Lấy một thanh sắt nặng 16,8 gam cho vào 2 lít dung dịch hỗn hợp AgNO3 0,2M và Cu(NO3)2 0,1M. Thanh sắt có tan hết không? Tính nồng độ mol của chất tan có trong dung dịch thu được sau phản ứng. Biết các phản ứng xảy ra hoàn toàn và thể tích dung dịch thay đổi không đáng kể
-

Có 5 lọ mất nhãn đựng 5 dung dịch: NaOH, KCl, MgCl2, CuCl2, AlCl3. Hãy nhận biết từng dung dịch trên mà không dùng thêm hóa chất khác. Viết các phương trình phản ứng xảy ra và cho biết thứ tự nhận biết các dung dịch là
-

Đốt cháy hoàn toàn 11,5 gam hỗn hợp chất hữu cơ X chứa (C, H, O) rồi hấp thụ hết sản phẩm cháy vào bình đựng dung dịch nước vôi trong. Sau thí nghiệm thấy khối lượng bình tăng thêm 35,5 gam. Lọc, thu được 28 gam chất kết tủa và dung dịch Y, đun kỹ dung dịch Y thu thêm được 11 gam kết tủa nữa. Xác định công thức phân tử, công thức cấu tạo của X. Biết MX < 78 đvC
-

Từ tinh bột, các hóa chất vô cơ và điều kiện cần thiết khác có đủ. Qua bao nhiêu phản ứng để điều chế được Etyl axetat? Viết phương trình hóa học (ghi rõ điều kiện nếu có)
-

Cho m gam Fe tác dụng hết với oxi thu được 44,8 gam hỗn hợp chất rắn A gồm 2 oxit (FeO, Fe2O3). Cho toàn bộ lượng hỗn hợp A trên tác dụng hết với dung dịch HNO3 (dư), thu được dung dịch B và 4,48 lít hỗn hợp khí C (đktc) gồm các sản phẩm khử là NO và NO2, tỉ khối của hỗn hợp C so với H2 là 1. Tính giá trị của m
-

Hòa tan Fe3O4 vào dung dịch H2SO4 (loãng, vừa đủ, không có không khí), thu được dung dịch A. Cho Cu (dư) vào dung dịch A, thu được dung dịch B. Thêm dung dịch NaOH (loãng, dư, không có không khí) vào dung dịch B, lọc lấy kết tủa đem nung trong không khí tới khối lượng không đổi. Có bao nhiêu phản ứng xảy ra? Viết các phương trình hóa học của các phản ứng đã xảy ra. Biết các phản ứng xảy ra hoàn toàn
-

Có 6 ống nghiệm bị mất nhãn được đánh số theo thứ tự từ 1 đến 6. Mỗi ống nghiệm đựng một trong các dung dịch sau: BaCl2, H2SO4, Ca(OH)2, MgCl2, Na2CO3, KHSO4. Hãy xác định dung dịch có trong mỗi ống nghiệm, viết các phương trình phản ứng hóa học xảy ra. Biết rằng khi tiến hành thí nghiệm thu được kết quả như sau:
- Dung dịch ở ống 2 cho kết tủa với các dung dịch ở ống 3 và 4
- Dung dịch ở ống 6 cho kết tủa với các dung dịch ở ống 1 và 4
- Dung dịch ở ống 4 cho khi bay lên khi tác dụng với các dung dịch ở ống 3 và 5
