Hỗn hợp khí X gồm 2 hidrocacbon A, B có công thức phân tử dạng CnH2n+2 hơn kém nhau một nhóm –CH2- trong phân tử và etilen. BIết rằng 4,48 lít khí X ở đktc làm mất màu vừa đủ dung dịch có chứa 8,0 gam brom. Trả lời câu hỏi dưới đây:Tính số mol của các chất tan có trong bình Y.

Câu hỏi
Nhận biếtHỗn hợp khí X gồm 2 hidrocacbon A, B có công thức phân tử dạng CnH2n+2 hơn kém nhau một nhóm –CH2- trong phân tử và etilen. BIết rằng 4,48 lít khí X ở đktc làm mất màu vừa đủ dung dịch có chứa 8,0 gam brom.
Trả lời câu hỏi dưới đây:
Tính số mol của các chất tan có trong bình Y.
Đáp án đúng: C
Lời giải của Luyện Tập 365
nX = 0, 1 mol =>Số mol C2H4 = 0,1 .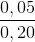 = 0,025 mol
= 0,025 mol
Gọi x,y lần lượt là số mol C2H6 và C3H8 có trong 0,1 mol X.
Dựa vào (2,3,4) và dữ kiện đề ra ta có:
x+ y = 0,075
(28.0,025) + 30x + 44y = 3,3
Giải ra được x = 0,05; y = 0,025
=>Số mol CO2 = 2. 0,025 + 2.0,05 + 3.0,025 = 0,225 mol
=>nNaOH : 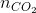 = 1,11
= 1,11
=>tạo 2 muối
NaOH + CO2 → NaHCO3 (5)
a a a
2NaOH + CO2 → Na2CO3 + H2O (6)
2b b b
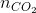 = a + b = 0,225
= a + b = 0,225
nNaOH = a + 2b = 0,25
giải ra được a = 0,05; b = 0,025
=>Số mol NaHCO3 = 0,05 mol; số mol Na2CO3 = 0,025 mol
nX = 0, 1 mol =>Số mol C2H4 = 0,1 .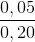 = 0,025 mol
= 0,025 mol
Gọi x,y lần lượt là số mol C2H6 và C3H8 có trong 0,1 mol X.
Dựa vào (2,3,4) và dữ kiện đề ra ta có:
x+ y = 0,075
(28.0,025) + 30x + 44y = 3,3
Giải ra được x = 0,05; y = 0,025
=>Số mol CO2 = 2. 0,025 + 2.0,05 + 3.0,025 = 0,225 mol
=>nNaOH : 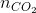 = 1,11
= 1,11
=>tạo 2 muối
NaOH + CO2 → NaHCO3 (5)
a a a
2NaOH + CO2 → Na2CO3 + H2O (6)
2b b b
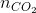 = a + b = 0,225
= a + b = 0,225
nNaOH = a + 2b = 0,25
giải ra được a = 0,05; b = 0,025
=>Số mol NaHCO3 = 0,05 mol; số mol Na2CO3 = 0,025 mol
Câu hỏi liên quan
-

Dẫn luồng khí CO dư qua hỗn hợp các chất: BaO, CuO, Fe3O4, Al2O3 nung nóng (các chất có số mol bằng nhau). Kết thúc các phản ứng thu được chất rắn X và khí Y. Cho X vào H2O (lấy dư) thu được dung dịch E và phần không tan Q. Cho Q vào dung dịch AgNO3 (số mol AgNO3 bằng hai lần tổng số mol các chất trong hỗn hợp ban đầu) thu được dung dịch T và chất rắn F. Lấy khí Y cho sục qua dung dịch T được dung dịch G và kết tủa H. Xác định thành phần các chất của X, Y, E, Q, F, T, G, H và viết các phương trình hóa học xảy ra
-

Cho m gam bột kim loại R có hóa trị không đổi vào 500ml dung dịch hỗn hợp gồm Cu(NO3)2 và AgNO3 đều có nồng độ 0,4M. Sau khi các phản ứng xảy ra hoàn toàn, thu được (m + 27,2) gam hỗn hợp rắn A và dung dịch Y. A tác dụng với dung dịch HCl có khí hydro thoát ra. Hãy xác định kim loại R và số mol muối tạo thành trong dung dịch Y
-

Hòa tan hoàn toàn 0,297 gam hỗn hợp Natri và một kim loại thuộc nhóm IIA trong bảng tuần hoàn các nguyên tố hóa học vào nước. Ta được dung dịch X và 56ml khí Y (đktc). Xác định kim loại thuộc nhóm IIA và khối lượng của mỗi kim loại trong hỗn hợp
-

Tính a
-

Chỉ dùng thêm thuốc thử duy nhất là dung dịch KOH, thứ tự nhận biết các dung dịch và nêu phương pháp phân biệt các dung dịch sau: Na2CO3, MgSO4, CH3COOH, C2H5OH
-

Có 5 lọ mất nhãn đựng 5 dung dịch: NaOH, KCl, MgCl2, CuCl2, AlCl3. Hãy nhận biết từng dung dịch trên mà không dùng thêm hóa chất khác. Viết các phương trình phản ứng xảy ra và cho biết thứ tự nhận biết các dung dịch là
-

Hòa tan Fe3O4 vào dung dịch H2SO4 (loãng, vừa đủ, không có không khí), thu được dung dịch A. Cho Cu (dư) vào dung dịch A, thu được dung dịch B. Thêm dung dịch NaOH (loãng, dư, không có không khí) vào dung dịch B, lọc lấy kết tủa đem nung trong không khí tới khối lượng không đổi. Có bao nhiêu phản ứng xảy ra? Viết các phương trình hóa học của các phản ứng đã xảy ra. Biết các phản ứng xảy ra hoàn toàn
-

Cho hỗn hợp A gồm các chất (K2O, Ca(NO3)2, NH4NO3, KHCO3) có số mol bằng nhau vào nước (dư), sau khi các phản ứng xảy ra hoàn toàn, đun nóng đến khi không còn khí thoát ra, thu được dung dịch B. Xác định chất tan và môi trường của dung dịch B
-

Viết các phương trình phản ứng xảy ra và tìm giá trị của a
-

Đốt cháy hoàn toàn 11,5 gam hỗn hợp chất hữu cơ X chứa (C, H, O) rồi hấp thụ hết sản phẩm cháy vào bình đựng dung dịch nước vôi trong. Sau thí nghiệm thấy khối lượng bình tăng thêm 35,5 gam. Lọc, thu được 28 gam chất kết tủa và dung dịch Y, đun kỹ dung dịch Y thu thêm được 11 gam kết tủa nữa. Xác định công thức phân tử, công thức cấu tạo của X. Biết MX < 78 đvC
