Dung dịch X gồm 0,1 mol H+, z mol Al3+, t mol NO3- và 0,02 mol SO42-. Cho 120ml dung dịch Y gồm KOH 1,2M và Ba(OH)2 0,1M vào X, sau khi các phản ứng kết thúc, thu được 3,732 gam kết tủa. Giá trị của z, t lần lượt là:

Câu hỏi
Nhận biếtDung dịch X gồm 0,1 mol H+, z mol Al3+, t mol NO3- và 0,02 mol SO42-. Cho 120ml dung dịch Y gồm KOH 1,2M và Ba(OH)2 0,1M vào X, sau khi các phản ứng kết thúc, thu được 3,732 gam kết tủa. Giá trị của z, t lần lượt là:
Đáp án đúng: C
Lời giải của Luyện Tập 365
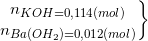 =>
=> 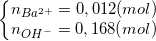
Áp dụng bảo toàn điện tích cho dung dịch Z, ta có:
0,1 + 3z = t + 0,04 <=> t - 3z = 0,06 (*)
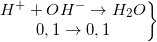 =>
=> 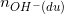 = 0,068 (mol)
= 0,068 (mol)
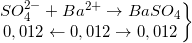 =>
=> 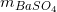 = 2,796 (gam)
= 2,796 (gam)
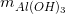 = 3,732 - 2,796 = 0,936 (gam) =>
= 3,732 - 2,796 = 0,936 (gam) => 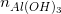 = 0,012 (mol)
= 0,012 (mol)
Vì 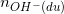 = 0,068 > 3
= 0,068 > 3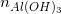 = 0,012 => Al3+ hết, một phần Al(OH)3 bị hoà tan
= 0,012 => Al3+ hết, một phần Al(OH)3 bị hoà tan
=> Dung dịch sau cùng: t mol NO3-; 0,144 mol K+; 0,008 mol SO42-và (z - 0,012) mol [Al(OH)4]-
Áp dụng bảo toàn điện tích cho dung dịch, ta có:
0,144 = t + 0,016 + (z - 0,012) <=> t + z = 0,14 (**)
Từ (*) và (**) => z = 0,02 (mol); t = 0,12 (mol) => Đáp án C
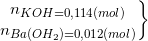 =>
=> 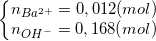
Áp dụng bảo toàn điện tích cho dung dịch Z, ta có:
0,1 + 3z = t + 0,04 <=> t - 3z = 0,06 (*)
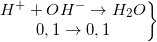 =>
=> 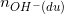 = 0,068 (mol)
= 0,068 (mol)
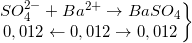 =>
=> 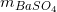 = 2,796 (gam)
= 2,796 (gam)
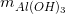 = 3,732 - 2,796 = 0,936 (gam) =>
= 3,732 - 2,796 = 0,936 (gam) => 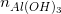 = 0,012 (mol)
= 0,012 (mol)
Vì 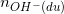 = 0,068 > 3
= 0,068 > 3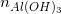 = 0,012 => Al3+ hết, một phần Al(OH)3 bị hoà tan
= 0,012 => Al3+ hết, một phần Al(OH)3 bị hoà tan
=> Dung dịch sau cùng: t mol NO3-; 0,144 mol K+; 0,008 mol SO42-và (z - 0,012) mol [Al(OH)4]-
Áp dụng bảo toàn điện tích cho dung dịch, ta có:
0,144 = t + 0,016 + (z - 0,012) <=> t + z = 0,14 (**)
Từ (*) và (**) => z = 0,02 (mol); t = 0,12 (mol) => Đáp án C
Câu hỏi liên quan
-

Đốt cháy hoàn toàn 0,1 mol este X thu được 0,3 mol khí CO2 và 0,3 mol H2O. Nếu cho 0,1 mol X tác dụng hết với NaOH thì thu được 8,2 gam muối. X là
-

Cho hỗn hợp X gồm ancol metylic, etylen glicol và glixeron. Đốt cháy hoàn toàn m gam X thu được 6,72 lít khí CO2 (đktc). Cũng m gam X trên cho tác dụng với Na dư thu được tối đa V lít khí H2 (đktc). Giá trị của V là
-

Cho các phương trình phản ứng: Fe + X → FeCl2 +... Chất X nào sau đây chọn không đúng?
-

Nung nóng m gam hỗn hợp gồm Al và Fe3O4 trong điều kiện không có không khí. Sau khi phản ứng xảy ra hoàn toàn thu được hỗn hợp rắn X. Cho X tác dụng với dung dịch NaOH (dư) thu được dung dịch Y, chất rắn Z và 3,36 lít khí H2 (ở đktc). Sục khí CO2 dư vào dung dịch Y, thu được 39 gam kết tủa. Giá trị của m là
-

Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai ancol đơn chức, cùng dãy đồng đẳng, thu được 15,68 lít CO2 (đktc) và 17,1 gam nước. Mặt khác, thực hiện phản ứng este hóa m gam X với 15,6 gam axit axetic, thu được a gam este. Biết hiệu suất phản ứng este hóa của hai ancol đều bằng 60%. Giá trị của a là
-

Hai chất được dùng để làm mềm nước cứng vĩnh cửu là:
-

Este X (MX =103 đvC) được điều chế từ một ancol đơn chức ( có tỉ khối hơi so với oxi lớn hơn 1) và một amino axit. Cho 25,75 gam X phản ứng hết với 300ml dung dich NaOH 1M, thu được dung dịch Y. Cô cạn Y thu được m gam chất rắn. Giá trị m là
-

Cho 21 gam hỗn hợp gồm glyxin và axit axetic tác dụng vừa đủ với dung dịch KOH, thu được dung dịch X chứa 32,4 gam muối. Cho X tác dụng với dung dịch HCl dư, thu được dung dịch chứa m gam muối. Giá trị của m là
-

Cho AgNO3 vào từng dung dịch NaF, NaCl, NaBr, NaI thì muối Halogen tạo được kết tủa là
-

Thêm rất từ từ dung dịch chứa 0,3 mol HCl vào 400ml dung dịch Na2CO3 0,5M đến khi kết thúc phản ứng thu được dung dịch X và khí Y. Thêm tiếp nước vôi trong dư vào dung dịch X, sau phản ứng khối lượng kết tủa thu được là
