Điện phân với 2 điện cực trơ một dung dịch chứa a gam CuSO4 cho tới khi có 0,448 lít khí (đo ở đktc) xuất hiện ở anot thì ngừng điện phân và thu được dung dịch X. Ngâm 1 lá sắt sạch trong X, kết thúc phản ứng lấy lá sắt ra, rửa sạch, làm khô, cân lại thấy khối lượng lá sắt không thay đổi. Giá trị của a là

Câu hỏi
Nhận biếtĐiện phân với 2 điện cực trơ một dung dịch chứa a gam CuSO4 cho tới khi có 0,448 lít khí (đo ở đktc) xuất hiện ở anot thì ngừng điện phân và thu được dung dịch X. Ngâm 1 lá sắt sạch trong X, kết thúc phản ứng lấy lá sắt ra, rửa sạch, làm khô, cân lại thấy khối lượng lá sắt không thay đổi. Giá trị của a là
Đáp án đúng: B
Lời giải của Luyện Tập 365
Các phản ứng điện cực :
+/ Anot : Cu+2 + 2e 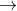 Cu
Cu
+/ Catot : 2H2O 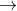 4H+ + O2 + 4e
4H+ + O2 + 4e
Do có H+ nên Fe tan 1 phần, tuy nhiên khối lượng thanh sắt không đổi sau phản ứng chứng tỏ Cu2+ vẫn dư và phản ứng.
Đặt số mol Cu2+ dư là x mol.
Có nO2 = 0,02 mol => nH+ = ne trao đổi = 0,08 mol
=>Xét thanh Fe : mgiảm = mtăng => 8x = 56.0,04 => x = 0,28 mol
=> nCuSO4 ban đầu = x + ½ ne trao đổi = 0,32 mol
=> a = 51,2g
=>B
Các phản ứng điện cực :
+/ Anot : Cu+2 + 2e 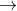 Cu
Cu
+/ Catot : 2H2O 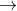 4H+ + O2 + 4e
4H+ + O2 + 4e
Do có H+ nên Fe tan 1 phần, tuy nhiên khối lượng thanh sắt không đổi sau phản ứng chứng tỏ Cu2+ vẫn dư và phản ứng.
Đặt số mol Cu2+ dư là x mol.
Có nO2 = 0,02 mol => nH+ = ne trao đổi = 0,08 mol
=>Xét thanh Fe : mgiảm = mtăng => 8x = 56.0,04 => x = 0,28 mol
=> nCuSO4 ban đầu = x + ½ ne trao đổi = 0,32 mol
=> a = 51,2g
=>B
Câu hỏi liên quan
-

Cho các chất sau C6H5-NH2 (X); Cl-C6H4 -NH2 (Y); O2N-C6H4 -NH2 (Z); CH3-C6H4-NH2 (T). Chất có tính bazơ mạnh nhất là:
-

Oxi hóa 4,48 lít C2H4 (ở đktc) bằng O2 (xúc tác PdCl2, CuCl2), thu được chất X đơn chức. Toàn bộ lượng chất X trên cho tác dụng với HCN (dư) thì được 7,1 gam CH3CH(CN)OH (Xianohiđrin). Hiệu suất quá trình tạo CH3CH(CN)OH từ C2H4 là
-

Cho AgNO3 vào từng dung dịch NaF, NaCl, NaBr, NaI thì muối Halogen tạo được kết tủa là
-

Cho các phương trình phản ứng: Fe + X → FeCl2 +... Chất X nào sau đây chọn không đúng?
-

Trong phân tử aminoaxit X có một nhóm amino và một nhóm cacboxyl. Cho 15,0 gam X tác dụng vừa đủ với dung dịch NaOH, cô cạn dung dịch sau phản ứng thu được 19,4 gam muối khan. Công thức của X là:
-

Nhận định nào dưới đây là đúng?
-

Este X (MX =103 đvC) được điều chế từ một ancol đơn chức ( có tỉ khối hơi so với oxi lớn hơn 1) và một amino axit. Cho 25,75 gam X phản ứng hết với 300ml dung dich NaOH 1M, thu được dung dịch Y. Cô cạn Y thu được m gam chất rắn. Giá trị m là
-

Hai chất được dùng để làm mềm nước cứng vĩnh cửu là:
-

Hợp chất X có công thức tổng quát (CxH4Ox)n thuộc loại axit no đa chức ,mạch hở. Giá trị của x là n tương ứng là
-

Trong công nghiệp, amoniac được điều chế từ nitơ và hiđrô bằng phương pháp tổng hợp: N2 (k) + 3H2 (k) <=> 2NH3 (k). Phản ứng theo chiều thuận là phản ứng tỏa nhiệt. Về lý thuyết, cân bằng trên sẽ dịch chuyển về phía tạo thành amoniac nếu
