Cho m gam hỗn hợp X gồm FeO, Fe2O3, Fe3O4 vào một lượng vừa đủ dung dịch HCl 2M, thu được dung dịch Y có tỉ lệ mol Fe2+ và Fe3+ là 1:2. Chia Y thành hai phần bằng nhau. Cô cạn phần 1 thu được m1 gam muối khan. Sục khí Clo dư vào phần 2, cô cạn dung dịch sau phản ứng thu được m2 gam muối khan. Biết m2 – m1 = 0,71. Thể tích dung dịch HCl đã dùng là

Câu hỏi
Nhận biếtCho m gam hỗn hợp X gồm FeO, Fe2O3, Fe3O4 vào một lượng vừa đủ dung dịch HCl 2M, thu được dung dịch Y có tỉ lệ mol Fe2+ và Fe3+ là 1:2. Chia Y thành hai phần bằng nhau. Cô cạn phần 1 thu được m1 gam muối khan. Sục khí Clo dư vào phần 2, cô cạn dung dịch sau phản ứng thu được m2 gam muối khan. Biết m2 – m1 = 0,71. Thể tích dung dịch HCl đã dùng là
Đáp án đúng: A
Lời giải của Luyện Tập 365
Quy đổi hỗn hợp X gồm FeO, Fe2O3, Fe3O4 thành hỗn hợp FeO, Fe2O3
FeO + 2HCl 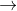 FeCl2 + H2O (1)
FeCl2 + H2O (1)
0,08 0,04
Fe2O3 + 6HCl 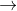 2FeCl3 + 3H2O (2)
2FeCl3 + 3H2O (2)
0,24 0,08
dd Y gồm : 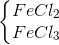
+) Phần 1: cô cạn m1 gam (FeCl2, FeCl3)
+) Phần 2: 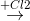 đem cô cạn
đem cô cạn  m2 gam FeCl3
m2 gam FeCl3
Áp dụng định luật bảo toàn khối lượng ta có:
mCl2 = m2 - m1 = 0,71 g => nCl2 = 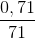 = 0,01 mol
= 0,01 mol
2FeCl2 + Cl2  2FeCl3
2FeCl3
0,02 0,01
Theo đề: 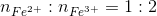 => nFeCl3 = 0,04 mol
=> nFeCl3 = 0,04 mol
Vậy dung dịch Y có 0,04 mol FeCl2 và 0,08 mol FeCl3
Theo PTPU (1) và (2) ta có: 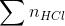 = 0,08 + 0,24 = 0,32 mol
= 0,08 + 0,24 = 0,32 mol
=> V dd HCl = 0,32 : 2 = 0,16 (lit) = 160 ml
=> Đáp án A
Quy đổi hỗn hợp X gồm FeO, Fe2O3, Fe3O4 thành hỗn hợp FeO, Fe2O3
FeO + 2HCl 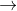 FeCl2 + H2O (1)
FeCl2 + H2O (1)
0,08 0,04
Fe2O3 + 6HCl 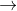 2FeCl3 + 3H2O (2)
2FeCl3 + 3H2O (2)
0,24 0,08
dd Y gồm : 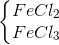
+) Phần 1: cô cạn m1 gam (FeCl2, FeCl3)
+) Phần 2: 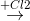 đem cô cạn
đem cô cạn 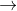 m2 gam FeCl3
m2 gam FeCl3
Áp dụng định luật bảo toàn khối lượng ta có:
mCl2 = m2 - m1 = 0,71 g => nCl2 = 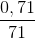 = 0,01 mol
= 0,01 mol
2FeCl2 + Cl2 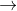 2FeCl3
2FeCl3
0,02 0,01
Theo đề: 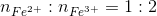 => nFeCl3 = 0,04 mol
=> nFeCl3 = 0,04 mol
Vậy dung dịch Y có 0,04 mol FeCl2 và 0,08 mol FeCl3
Theo PTPU (1) và (2) ta có: 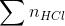 = 0,08 + 0,24 = 0,32 mol
= 0,08 + 0,24 = 0,32 mol
=> V dd HCl = 0,32 : 2 = 0,16 (lit) = 160 ml
=> Đáp án A
Câu hỏi liên quan
-

Hòa tan hết 7,2 gam hỗn hợp X gồm hai muối cacbonat của hai kim loại kế tiếp nhau trong nhóm IIA bằng dung dịch H2SO4 loãng, thu được khí Y. Cho toàn bộ khí Y hấp thụ hết bởi dung dịch Ba(OH)2 dư thu được 15,76 gam kết tủa. Hai kim loại ban đầu là
-

Cho AgNO3 vào từng dung dịch NaF, NaCl, NaBr, NaI thì muối Halogen tạo được kết tủa là
-

Thêm rất từ từ dung dịch chứa 0,3 mol HCl vào 400ml dung dịch Na2CO3 0,5M đến khi kết thúc phản ứng thu được dung dịch X và khí Y. Thêm tiếp nước vôi trong dư vào dung dịch X, sau phản ứng khối lượng kết tủa thu được là
-

Đốt cháy hoàn toàn 0,1 mol este X thu được 0,3 mol khí CO2 và 0,3 mol H2O. Nếu cho 0,1 mol X tác dụng hết với NaOH thì thu được 8,2 gam muối. X là
-

Nhận định nào dưới đây là đúng?
-

Chia m gam hỗn hợp gồm Na2O và Al2O3 thành 2 phần đều nhau: - Phần 1: Hòa tan trong nước dư thu được 1,02 gam chất rắn không tan - Phần 2: Hòa tan hết trong dung dịch HCl 1M thì cần vừa đủ 140ml dung dịch HCl. Khối lượng hỗn hợp ban đầu m có giá trị bằng
-

Hòa tan hoàn toàn 0,3 mol hỗn hợp gồm Al và Al4C3 vào dung dịch KOH (dư), thu được a mol hỗn hợp khí và dung dịch X. Sục khí CO2 (dư) vào dung dịch X, lượng kết tủa thu được là 46,8 gam. Giá trị của a là
-

Trong các chất HF, HCl, HBr và HI thì
-

Cho các chất sau C6H5-NH2 (X); Cl-C6H4 -NH2 (Y); O2N-C6H4 -NH2 (Z); CH3-C6H4-NH2 (T). Chất có tính bazơ mạnh nhất là:
-

Nung nóng m gam hỗn hợp gồm Al và Fe3O4 trong điều kiện không có không khí. Sau khi phản ứng xảy ra hoàn toàn thu được hỗn hợp rắn X. Cho X tác dụng với dung dịch NaOH (dư) thu được dung dịch Y, chất rắn Z và 3,36 lít khí H2 (ở đktc). Sục khí CO2 dư vào dung dịch Y, thu được 39 gam kết tủa. Giá trị của m là
