Cho hỗn hợp Mg và Fe. Chia hỗn hợp làm hai phần bằng nhau: - Phần 1: Đốt cháy trong khí O2 tạo thành 50,8 gam hỗn hợp các oxit, cho hỗn hợp này tác dụng với dung dịch HNO3 dư, tạo thành 1,12 lít khí NO (là sản phẩm khử duy nhất). - Phần 2: Đốt cháy trong khí CO2 dư, tạo thành 42,4 gam hỗn hợp rắn X. Hòa tan hoàn toàn X trong dung dịch HNO3 dư, thu được V lít khí NO (sản phẩm khử duy nhất).Giá trị của V là:

Câu hỏi
Nhận biếtCho hỗn hợp Mg và Fe. Chia hỗn hợp làm hai phần bằng nhau: - Phần 1: Đốt cháy trong khí O2 tạo thành 50,8 gam hỗn hợp các oxit, cho hỗn hợp này tác dụng với dung dịch HNO3 dư, tạo thành 1,12 lít khí NO (là sản phẩm khử duy nhất). - Phần 2: Đốt cháy trong khí CO2 dư, tạo thành 42,4 gam hỗn hợp rắn X. Hòa tan hoàn toàn X trong dung dịch HNO3 dư, thu được V lít khí NO (sản phẩm khử duy nhất).Giá trị của V là:
Đáp án đúng: B
Lời giải của Luyện Tập 365
-Với phần thứ nhất: Coi các oxit gồm: MgO, FeO và Fe2O3 (Fe3O4 <=> FeO.Fe2O3)
=> nFeO=3nNO = 0,15 (mol)
- Với phần thứ hai: Khi đốt trong CO2, chỉ có Mg phản ứng (Mg + CO2 MgO + CO)
MgO + CO)
Coi các oxit gồm: MgO, FeO và Fe2O3 (Fe3O4 <=> FeO.Fe2O3)
=>mO(trong hai oxit sắt) =50,8- 42,4 = 8,4 (gam) => nO(trong hai oxit sắt) = 0,525 (mol)
- Áp dụng bảo toàn nguyên tố đối với oxi: 0,15 + 3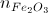 = 0,525
= 0,525
=>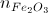 = 0125 (mol)
= 0125 (mol)
- Áp dụng bảo toàn nguyên tố đối với Fe: nFe(1 phần)= 0,15 + 0,125x2= 0,4 (mol)
- Khi tác dụng với HNO3 ở phần hai, quá trình nhường và nhận có số electron như nhau (3e)
=>nNO=nFe=0,4 (mol) => V = 8,96 (lít)
-Với phần thứ nhất: Coi các oxit gồm: MgO, FeO và Fe2O3 (Fe3O4 <=> FeO.Fe2O3)
=> nFeO=3nNO = 0,15 (mol)
- Với phần thứ hai: Khi đốt trong CO2, chỉ có Mg phản ứng (Mg + CO2 MgO + CO)
MgO + CO)
Coi các oxit gồm: MgO, FeO và Fe2O3 (Fe3O4 <=> FeO.Fe2O3)
=>mO(trong hai oxit sắt) =50,8- 42,4 = 8,4 (gam) => nO(trong hai oxit sắt) = 0,525 (mol)
- Áp dụng bảo toàn nguyên tố đối với oxi: 0,15 + 3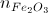 = 0,525
= 0,525
=>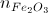 = 0125 (mol)
= 0125 (mol)
- Áp dụng bảo toàn nguyên tố đối với Fe: nFe(1 phần)= 0,15 + 0,125x2= 0,4 (mol)
- Khi tác dụng với HNO3 ở phần hai, quá trình nhường và nhận có số electron như nhau (3e)
=>nNO=nFe=0,4 (mol) => V = 8,96 (lít)
Câu hỏi liên quan
-

Nung nóng m gam hỗn hợp gồm Al và Fe3O4 trong điều kiện không có không khí. Sau khi phản ứng xảy ra hoàn toàn thu được hỗn hợp rắn X. Cho X tác dụng với dung dịch NaOH (dư) thu được dung dịch Y, chất rắn Z và 3,36 lít khí H2 (ở đktc). Sục khí CO2 dư vào dung dịch Y, thu được 39 gam kết tủa. Giá trị của m là
-

Cho AgNO3 vào từng dung dịch NaF, NaCl, NaBr, NaI thì muối Halogen tạo được kết tủa là
-

Có hai hi đrocacbon A, B đều là chất khí ở điều kiện thường, không phải là đồng phân của nhau.Khi đốt cháy hoàn toàn, mỗi chất đều tạo ra số mol nước gấp 3 lần số mol mỗi chất đã cháy. A và B thỏa mãn sơ đồ chuyển hóa sau: A
![\xrightarrow[600^{0}C]{Fe}](https://luyentap365.com/wp-content/picture/learning/exam/2013/1101/164_230_1.gif) X → Y → B → Cao su buna. Trong đó X, Y có cùng số lượng nguyên tử cacbon trong phân tử. Vậy Y là
X → Y → B → Cao su buna. Trong đó X, Y có cùng số lượng nguyên tử cacbon trong phân tử. Vậy Y là -

Cho các phương trình phản ứng: Fe + X → FeCl2 +... Chất X nào sau đây chọn không đúng?
-

Công thức hóa học của clorua vôi là
-

Cho hỗn hợp X gồm ancol metylic, etylen glicol và glixeron. Đốt cháy hoàn toàn m gam X thu được 6,72 lít khí CO2 (đktc). Cũng m gam X trên cho tác dụng với Na dư thu được tối đa V lít khí H2 (đktc). Giá trị của V là
-

Hai chất được dùng để làm mềm nước cứng vĩnh cửu là:
-

Dung dịch NaHCO3 trong nước
-

Đun nóng xenlulozơ với hỗn hợp HNO3 và H2SO4 đặc, thu được chất dễ cháy, nổ mạnh không có khói nên được dùng làm thuốc súng không khói. Sản phẩm đó là
-

Hòa tan 7,02 gam hỗn hợp gồm mantozơ và glucozơ vào nước rồi cho tác dụng hết với dung dịch AgNO3 dư trong NH3 thu được 6,48 gam Ag. Phần trăm theo khối lượng của glucozơ trong hỗn hợp ban đầu là
