Cho 2,13 gam P2O5 tác dụng với 80 ml dung dịch NaOH 1M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X chứa m gam muối. Bỏ qua sự thủy phân của các ion, giá trị của m là

Câu hỏi
Nhận biếtCho 2,13 gam P2O5 tác dụng với 80 ml dung dịch NaOH 1M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X chứa m gam muối. Bỏ qua sự thủy phân của các ion, giá trị của m là
Đáp án đúng: A
Lời giải của Luyện Tập 365
Có nP2O5 = 0,015 mol ; nNaOH = 0,08 mol
Ta thấy 4nP2O5 < nNaOH < 6nP2O5
=> Các phản ứng xảy ra là :
+/ 4NaOH + P2O5 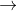 2Na2HPO4 + H2O
2Na2HPO4 + H2O
Mol 4x x 2x
+/ 6NaOH + P2O5 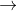 2Na3PO4 + 3H2O
2Na3PO4 + 3H2O
Mol 6y y 2y
=> Có nNaOH = x + y = 0,015 mol
Và nP2O5 = 4x + 6y = 0,08 mol
=> x = 0,005 mol ; y = 0,01 mol
=> m = mNa2HPO4 + mNa3PO4 = 4,7g
=>A
Có nP2O5 = 0,015 mol ; nNaOH = 0,08 mol
Ta thấy 4nP2O5 < nNaOH < 6nP2O5
=> Các phản ứng xảy ra là :
+/ 4NaOH + P2O5 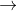 2Na2HPO4 + H2O
2Na2HPO4 + H2O
Mol 4x x 2x
+/ 6NaOH + P2O5 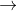 2Na3PO4 + 3H2O
2Na3PO4 + 3H2O
Mol 6y y 2y
=> Có nNaOH = x + y = 0,015 mol
Và nP2O5 = 4x + 6y = 0,08 mol
=> x = 0,005 mol ; y = 0,01 mol
=> m = mNa2HPO4 + mNa3PO4 = 4,7g
=>A
Câu hỏi liên quan
-

Hòa tan hết 7,2 gam hỗn hợp X gồm hai muối cacbonat của hai kim loại kế tiếp nhau trong nhóm IIA bằng dung dịch H2SO4 loãng, thu được khí Y. Cho toàn bộ khí Y hấp thụ hết bởi dung dịch Ba(OH)2 dư thu được 15,76 gam kết tủa. Hai kim loại ban đầu là
-

Thêm rất từ từ dung dịch chứa 0,3 mol HCl vào 400ml dung dịch Na2CO3 0,5M đến khi kết thúc phản ứng thu được dung dịch X và khí Y. Thêm tiếp nước vôi trong dư vào dung dịch X, sau phản ứng khối lượng kết tủa thu được là
-

Trong công nghiệp, amoniac được điều chế từ nitơ và hiđrô bằng phương pháp tổng hợp: N2 (k) + 3H2 (k) <=> 2NH3 (k). Phản ứng theo chiều thuận là phản ứng tỏa nhiệt. Về lý thuyết, cân bằng trên sẽ dịch chuyển về phía tạo thành amoniac nếu
-

Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai ancol đơn chức, cùng dãy đồng đẳng, thu được 15,68 lít CO2 (đktc) và 17,1 gam nước. Mặt khác, thực hiện phản ứng este hóa m gam X với 15,6 gam axit axetic, thu được a gam este. Biết hiệu suất phản ứng este hóa của hai ancol đều bằng 60%. Giá trị của a là
-

Hòa tan 7,02 gam hỗn hợp gồm mantozơ và glucozơ vào nước rồi cho tác dụng hết với dung dịch AgNO3 dư trong NH3 thu được 6,48 gam Ag. Phần trăm theo khối lượng của glucozơ trong hỗn hợp ban đầu là
-

Có hai hi đrocacbon A, B đều là chất khí ở điều kiện thường, không phải là đồng phân của nhau.Khi đốt cháy hoàn toàn, mỗi chất đều tạo ra số mol nước gấp 3 lần số mol mỗi chất đã cháy. A và B thỏa mãn sơ đồ chuyển hóa sau: A
![\xrightarrow[600^{0}C]{Fe}](https://luyentap365.com/wp-content/picture/learning/exam/2013/1101/164_230_1.gif) X → Y → B → Cao su buna. Trong đó X, Y có cùng số lượng nguyên tử cacbon trong phân tử. Vậy Y là
X → Y → B → Cao su buna. Trong đó X, Y có cùng số lượng nguyên tử cacbon trong phân tử. Vậy Y là -

Hiđrocacbon X có khối lượng mol bằng 100 gam. Cho X tác dụng với clo tạo ra hỗn hợp 3 dẫn xuất monoclo là đồng phân của nhau. Có bao nhiêu chất X thỏa mãn điều kiện trên?
-

Đốt cháy hoàn toàn 0,1 mol este X thu được 0,3 mol khí CO2 và 0,3 mol H2O. Nếu cho 0,1 mol X tác dụng hết với NaOH thì thu được 8,2 gam muối. X là
-

Este X (MX =103 đvC) được điều chế từ một ancol đơn chức ( có tỉ khối hơi so với oxi lớn hơn 1) và một amino axit. Cho 25,75 gam X phản ứng hết với 300ml dung dich NaOH 1M, thu được dung dịch Y. Cô cạn Y thu được m gam chất rắn. Giá trị m là
-

Khối lượng của tinh bột cần dùng trong quá trình lên men để tạo thành 5 lít ancol etylic 460 là (biết hiệu suất của cả quá trình là 72% và khối lượng riêng của ancol là 0,8g/ml)
