Cho hỗn hợp X gồm CuO và NaOH có tỉ lệ số mol 1:1 tác dụng vừa đủ với dung dịch hỗn hợp HCl 1M và H2SO4 0,5M thu được dung dịch Y chỉ chứa m gam hỗn hợp muối trung hoà . Điện phân dung dịch Y với điện cực trơ màng ngăn xốp cường độ I=2,68A đến khi khối lượng dung dịch giảm 20,225 gam mất t giây thì dừng lại thu được dung dịch Z. Cho m gam Fe vào dung dịch Z sau khi phản ứng kết thúc thu được 0,9675m gam hỗn hợp 2 kim loại. Giá trị của t là

Câu hỏi
Nhận biếtCho hỗn hợp X gồm CuO và NaOH có tỉ lệ số mol 1:1 tác dụng vừa đủ với dung dịch hỗn hợp HCl 1M và H2SO4 0,5M thu được dung dịch Y chỉ chứa m gam hỗn hợp muối trung hoà . Điện phân dung dịch Y với điện cực trơ màng ngăn xốp cường độ I=2,68A đến khi khối lượng dung dịch giảm 20,225 gam mất t giây thì dừng lại thu được dung dịch Z. Cho m gam Fe vào dung dịch Z sau khi phản ứng kết thúc thu được 0,9675m gam hỗn hợp 2 kim loại. Giá trị của t là
Đáp án đúng: A
Lời giải của Luyện Tập 365
Đặt số mol mỗi chất trong X là a mol
Dung dịch axit có CHCl = 2CH2SO4
=> nCl = 2nSO4
=>Khi phản ứng tạo muối trung hòa nên trong dung dịch có : Cu2+ ; Na+ ; Cl- ; SO42-
=> Bảo toàn điện tích : 2a + a = nCl + 2nSO4 = 4nSO4
=> nSO4 = 0,75a ; nCl = 1,5a
=> m = 64a + 23a + 96.0,75a + 35,5.1,5a
= 212,25a (*)
Khi cho Fe vào Z tạo hỗn hợp kim loại và khối lượng giảm so với ban đầu
=> Fe bị hòa tan 1 phần bởi H+ và Cu2+ dư
Khi điện phân : +/ Catot : Cu2+ + 2e 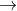 Cu
Cu
+/ Anot : 2Cl- 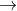 Cl2 + 2e
Cl2 + 2e
2H2O 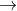 4H+ + O2 + 4e
4H+ + O2 + 4e
Đặt nO2 = b mol
Bảo toàn e => nCu2+ phản ứng = 0,75a + 2b => nCu2+ dư = 0,25a – 2b mol
=> mgiảm = mO2 + mCl2 + mCu = 32b + 71.0,75a + 64(0,75a + 2b) = 20,225 g
=> 101,25a + 160b = 20,225 (1)
Khi Cho Fe vào : Fe + 2H+ 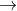 Fe2+ + H2
Fe2+ + H2
Fe + Cu2+ 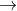 Fe2+ + Cu
Fe2+ + Cu
=> mgiảm = mFe phản ứng – mCu tạo ra
=> m – 0,9675m = 56.(2b + 0,25a – 2b ) – 64(0,25a – 2b)
=> 0,0325m = 128b – 2a (**)
Tử (*) và (**) => b = 14,39a (2)
Từ (1) và (2) => a = 0,18 mol ; b = 0,0125 mol
=> ne trao đổi = 2nCu2+ bị điện phân = 0,32 mol
=> t = 11523 s
=>A
Đặt số mol mỗi chất trong X là a mol
Dung dịch axit có CHCl = 2CH2SO4
=> nCl = 2nSO4
=>Khi phản ứng tạo muối trung hòa nên trong dung dịch có : Cu2+ ; Na+ ; Cl- ; SO42-
=> Bảo toàn điện tích : 2a + a = nCl + 2nSO4 = 4nSO4
=> nSO4 = 0,75a ; nCl = 1,5a
=> m = 64a + 23a + 96.0,75a + 35,5.1,5a
= 212,25a (*)
Khi cho Fe vào Z tạo hỗn hợp kim loại và khối lượng giảm so với ban đầu
=> Fe bị hòa tan 1 phần bởi H+ và Cu2+ dư
Khi điện phân : +/ Catot : Cu2+ + 2e 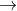 Cu
Cu
+/ Anot : 2Cl- 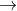 Cl2 + 2e
Cl2 + 2e
2H2O 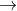 4H+ + O2 + 4e
4H+ + O2 + 4e
Đặt nO2 = b mol
Bảo toàn e => nCu2+ phản ứng = 0,75a + 2b => nCu2+ dư = 0,25a – 2b mol
=> mgiảm = mO2 + mCl2 + mCu = 32b + 71.0,75a + 64(0,75a + 2b) = 20,225 g
=> 101,25a + 160b = 20,225 (1)
Khi Cho Fe vào : Fe + 2H+ 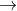 Fe2+ + H2
Fe2+ + H2
Fe + Cu2+ 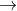 Fe2+ + Cu
Fe2+ + Cu
=> mgiảm = mFe phản ứng – mCu tạo ra
=> m – 0,9675m = 56.(2b + 0,25a – 2b ) – 64(0,25a – 2b)
=> 0,0325m = 128b – 2a (**)
Tử (*) và (**) => b = 14,39a (2)
Từ (1) và (2) => a = 0,18 mol ; b = 0,0125 mol
=> ne trao đổi = 2nCu2+ bị điện phân = 0,32 mol
=> t = 11523 s
=>A
Câu hỏi liên quan
-

Trong các chất HF, HCl, HBr và HI thì
-

Cho các chất sau C6H5-NH2 (X); Cl-C6H4 -NH2 (Y); O2N-C6H4 -NH2 (Z); CH3-C6H4-NH2 (T). Chất có tính bazơ mạnh nhất là:
-

Thêm rất từ từ dung dịch chứa 0,3 mol HCl vào 400ml dung dịch Na2CO3 0,5M đến khi kết thúc phản ứng thu được dung dịch X và khí Y. Thêm tiếp nước vôi trong dư vào dung dịch X, sau phản ứng khối lượng kết tủa thu được là
-

Chia m gam hỗn hợp gồm Na2O và Al2O3 thành 2 phần đều nhau: - Phần 1: Hòa tan trong nước dư thu được 1,02 gam chất rắn không tan - Phần 2: Hòa tan hết trong dung dịch HCl 1M thì cần vừa đủ 140ml dung dịch HCl. Khối lượng hỗn hợp ban đầu m có giá trị bằng
-

Cho hỗn hợp X gồm ancol metylic, etylen glicol và glixeron. Đốt cháy hoàn toàn m gam X thu được 6,72 lít khí CO2 (đktc). Cũng m gam X trên cho tác dụng với Na dư thu được tối đa V lít khí H2 (đktc). Giá trị của V là
-

Có hai hi đrocacbon A, B đều là chất khí ở điều kiện thường, không phải là đồng phân của nhau.Khi đốt cháy hoàn toàn, mỗi chất đều tạo ra số mol nước gấp 3 lần số mol mỗi chất đã cháy. A và B thỏa mãn sơ đồ chuyển hóa sau: A
![\xrightarrow[600^{0}C]{Fe}](https://luyentap365.com/wp-content/picture/learning/exam/2013/1101/164_230_1.gif) X → Y → B → Cao su buna. Trong đó X, Y có cùng số lượng nguyên tử cacbon trong phân tử. Vậy Y là
X → Y → B → Cao su buna. Trong đó X, Y có cùng số lượng nguyên tử cacbon trong phân tử. Vậy Y là -

Dung dịch NaHCO3 trong nước
-

Cho 21 gam hỗn hợp gồm glyxin và axit axetic tác dụng vừa đủ với dung dịch KOH, thu được dung dịch X chứa 32,4 gam muối. Cho X tác dụng với dung dịch HCl dư, thu được dung dịch chứa m gam muối. Giá trị của m là
-

Đốt cháy hoàn toàn 0,1 mol este X thu được 0,3 mol khí CO2 và 0,3 mol H2O. Nếu cho 0,1 mol X tác dụng hết với NaOH thì thu được 8,2 gam muối. X là
-

Công thức hóa học của clorua vôi là
