Hoà tan hoàn toàn 10,44 gam một oxit sắt bằng dung dịch H2SO4 đặc nóng thu được dung dịch X và 1,624 lít khí SO2 (sản phẩm khử duy nhất ở điều kiện tiêu chuẩn). cô cạn dung dịch X, thu được m gam muối sunfat khan. Giá trị của m là:

Câu hỏi
Nhận biếtHoà tan hoàn toàn 10,44 gam một oxit sắt bằng dung dịch H2SO4 đặc nóng thu được dung dịch X và 1,624 lít khí SO2 (sản phẩm khử duy nhất ở điều kiện tiêu chuẩn). cô cạn dung dịch X, thu được m gam muối sunfat khan. Giá trị của m là:
Đáp án đúng: A
Lời giải của Luyện Tập 365
Theo giả thiết ta có: X + H2SO4 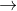 Fe2(SO4)3 + SO2 + H2O (1)
Fe2(SO4)3 + SO2 + H2O (1)
Ta quy đổi phản ứng trên thành:
X + O2 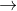 Fe2O3 (2)
Fe2O3 (2)
Nhận thấy sau các phản ứng (1) và (2), fe đều có số oxi hoá là +3 nên số mol electron mà X cho h2SO4 bằng số mol eletron mà X cho O2
=> 2.nSO2 = 4.nO2 => nO2 = 0,03625 mol
=> mO2 = 0,03625.32 = 1,16 gam
Theo định luật bảo toàn khối lượng ta có: mFe2O3 = mX + mO2 = 1,16 gam
=> nFe2O3 = 0,0725 mol
Do nguyên tố được bảo toàn nên nFe2(SO4)3 = nFe2O3 = 0,0725 mol
Vậy m = mFe2(SO4)3 = 0,0725.400 = 29 gam
=> Đáp án A
Theo giả thiết ta có: X + H2SO4 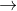 Fe2(SO4)3 + SO2 + H2O (1)
Fe2(SO4)3 + SO2 + H2O (1)
Ta quy đổi phản ứng trên thành:
X + O2 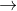 Fe2O3 (2)
Fe2O3 (2)
Nhận thấy sau các phản ứng (1) và (2), fe đều có số oxi hoá là +3 nên số mol electron mà X cho h2SO4 bằng số mol eletron mà X cho O2
=> 2.nSO2 = 4.nO2 => nO2 = 0,03625 mol
=> mO2 = 0,03625.32 = 1,16 gam
Theo định luật bảo toàn khối lượng ta có: mFe2O3 = mX + mO2 = 1,16 gam
=> nFe2O3 = 0,0725 mol
Do nguyên tố được bảo toàn nên nFe2(SO4)3 = nFe2O3 = 0,0725 mol
Vậy m = mFe2(SO4)3 = 0,0725.400 = 29 gam
=> Đáp án A
Câu hỏi liên quan
-

Cho các phương trình phản ứng: Fe + X → FeCl2 +... Chất X nào sau đây chọn không đúng?
-

Dung dịch NaHCO3 trong nước
-

Trong các chất HF, HCl, HBr và HI thì
-

Cho 21 gam hỗn hợp gồm glyxin và axit axetic tác dụng vừa đủ với dung dịch KOH, thu được dung dịch X chứa 32,4 gam muối. Cho X tác dụng với dung dịch HCl dư, thu được dung dịch chứa m gam muối. Giá trị của m là
-

Hợp chất X có công thức tổng quát (CxH4Ox)n thuộc loại axit no đa chức ,mạch hở. Giá trị của x là n tương ứng là
-

Nung nóng một hỗn hợp gồm CaCO3 và MgO tới khối lượng không đổi, thì số gam chất rắn còn lại chỉ bằng
 số gam hỗn hợp trước khi nung. Vậy % theo khối lượng của CaCO3 trong hỗn hợp ban đầu là
số gam hỗn hợp trước khi nung. Vậy % theo khối lượng của CaCO3 trong hỗn hợp ban đầu là -

Chia m gam hỗn hợp gồm Na2O và Al2O3 thành 2 phần đều nhau: - Phần 1: Hòa tan trong nước dư thu được 1,02 gam chất rắn không tan - Phần 2: Hòa tan hết trong dung dịch HCl 1M thì cần vừa đủ 140ml dung dịch HCl. Khối lượng hỗn hợp ban đầu m có giá trị bằng
-

Hòa tan hoàn toàn 0,3 mol hỗn hợp gồm Al và Al4C3 vào dung dịch KOH (dư), thu được a mol hỗn hợp khí và dung dịch X. Sục khí CO2 (dư) vào dung dịch X, lượng kết tủa thu được là 46,8 gam. Giá trị của a là
-

Do có tác dụng diệt khuẩn, đặc biệt là vi khuẩn gây thối rữa nên dung dịch của hợp chất X được dùng để ngâm xác động vật, thuộc da, tấy uế... X là
-

Đốt cháy hoàn toàn 0,3 gam hợp chất X có tỉ khối hơi so với hiđro bằng 30, sản phẩm tạo ra chỉ gồm 224ml khí CO2 (đktc) và 0,18 gam H20. Chất X vừa phản ứng được với NaOH, vừa có phản ứng tráng gương. Vậy X là
