(1đ). Viết công thức cấu tạo đầy đủ và công thức cấu tạo thu gọn, thu gọn nhất của các chất: etilen (C2H4); etanol (C2H5OH).

Câu hỏi
Nhận biết(1đ).
Viết công thức cấu tạo đầy đủ và công thức cấu tạo thu gọn, thu gọn nhất của các chất: etilen (C2H4); etanol (C2H5OH).
Đáp án đúng:
Lời giải của Luyện Tập 365
Công thức:
H-(H)C=C(H)-H và CH3-CH2-O-H
Áp dụng định nghĩa về công thức cấu tạo đầy đủ, công thức cấu tạo thu gọn và thu gọn nhất (sgk) để viết.
Công thức:
H-(H)C=C(H)-H và CH3-CH2-O-H
Áp dụng định nghĩa về công thức cấu tạo đầy đủ, công thức cấu tạo thu gọn và thu gọn nhất (sgk) để viết.
Câu hỏi liên quan
-

(1,5đ).
Viết các phương trình hoá học (ghi rõ điều kiện – nếu có) để hoàn thành sơ đồ phản ứng sau:
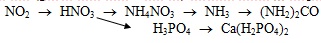
-

(1đ)
Cho Kb của CH3COO- ở 25oC là 5,56x10-10. Tính pH của dung dịch CH3COONa 0,5M ở 25oC.
-

(3 điểm):
a. Cho 16 gam Fe2O3 tác dụng vừa đủ với V ml dung dịch HNO3 1,5M, thu được dung dịch chứa a gam muối. Viết phương trình phản ứng xảy ra, tìm các giá trị V và a.
b. Hòa tan hoàn toàn 4,86 gam kim loại Al vào dung dịch HNO3 loãng, dư, thấy thoát ra 2,24 lít khí NO (ở đktc và là khí thoát ra duy nhất), tính khối lượng muối tan có trong dung dịch sau phản ứng.
-

(1,5đ)
Cho dung dịch HNO3 loãng lần lượt tác dụng với: Al(OH)3; kim loại Zn (N2O là sản phẩm khử duy nhất).
Viết các phương trình hoá học dưới dạng phân tử và ion thu gọn. Nêu vai trò của HNO3 trong mỗi phản ứng.
-

(3 điểm):
a. Cho 16,05 gam Fe(OH)3 tác dụng vừa đủ với V ml dung dịch HNO3 1M, thu được dung dịch chứa a gam muối. Viết phương trình phản ứng xảy ra, tìm các giá trị V và a.
b. Hòa tan hoàn toàn 10,08 gam kim loại Mg vào dung dịch HNO3 loãng, dư, thấy thoát ra 4,48 lít khí NO (ở đktc và là khí thoát ra duy nhất), tính khối lượng muối tan có trong dung dịch sau phản ứng.
-

(1,5đ)
Khi hoà tan 18 gam hỗn hợp X gồm Al và Mg vào dung dịch HNO3 loãng vừa đủ thì thu được 2,24 lít (đktc) khí N2O và dung dịch Y. Cho dung dịch NaOH dư vào dung dịch Y đun nhẹ thấy có 2,8 lít khí NH3 (đktc) thoát ra.
Viết các phương trình hoá học và tính số gam mỗi kim loại có trong X.
-

(1,5đ)
Viết các phương trình hoá học (ghi rõ điều kiện – nếu có) để hoàn thành sơ đồ phản ứng sau:
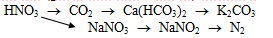
-

(1,5đ)
Dung dịch A gồm NaOH 0,8M và Ba(OH)2 0,6M. Dung dịch B (gồm HCl 0,04M và H2SO4) có pH = 1. Thêm V ml dung dịch B vào 100 ml dung dịch A để được dung dịch X có pH bằng 13. (coi thể tích dung dịch X bằng tổng thể tích dung dịch A và dung dịch B)
Tính V. Tính số gam kết tủa sinh ra trong thí nghiệm trên.
-

(4 điểm): Hoàn thành phương trình phân tử, viết phương trình ion thu gọn:
a. NaOH + HNO3
b. AgNO3 + NaCl
c. MgO + H2SO4
d. (NH4)2CO3 + HCl
-

(1,5đ)
Dung dịch A gồm NaOH 0,4M và Ba(OH)2 0,2M. Dung dịch B (gồm HCl 0,06M và H2SO4) có pH = 1. Thêm V ml dung dịch B vào 100 ml dung dịch A được dung dịch X có pH bằng 13. (coi thể tích dung dịch X bằng tổng thể tích dung dịch A và dung dịch B)
Tính V. Cô cạn dung dịch X được bao nhiêu gam chất rắn khan?
