(3 điểm): a. Hoàn thành sơ đồ sau bằng các phương trình phản ứng:
Cu  Cu(NO3)2
Cu(NO3)2  NO2
NO2  HNO3
b. Phân biệt 3 dung dịch riêng biệt sau bằng phương pháp hoá học:
(NH4)2CO3, NH4Cl, (NH4)2SO4
HNO3
b. Phân biệt 3 dung dịch riêng biệt sau bằng phương pháp hoá học:
(NH4)2CO3, NH4Cl, (NH4)2SO4

Câu hỏi
Nhận biết(3 điểm): a. Hoàn thành sơ đồ sau bằng các phương trình phản ứng:
Cu  Cu(NO3)2
Cu(NO3)2  NO2
NO2  HNO3
HNO3
b. Phân biệt 3 dung dịch riêng biệt sau bằng phương pháp hoá học:
(NH4)2CO3, NH4Cl, (NH4)2SO4
Đáp án đúng:
Lời giải của Luyện Tập 365
a.
(1) 3Cu + 8HNO3  3Cu(NO3)2 + 2NO + 4H2O
3Cu(NO3)2 + 2NO + 4H2O
Hoặc: Cu + 4HNO3  Cu(NO3)2 + 2NO2 + 2H2O
Cu(NO3)2 + 2NO2 + 2H2O
(2) 2Cu(NO3)2 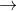 2CuO + 4NO2 + O2
2CuO + 4NO2 + O2
(3) 4NO2 + O2 + 2H2O 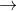 4HNO3
4HNO3
b.
* Dùng dung dịch HCl làm thuốc thử:
- Nhận ra dung dịch (NH4)2CO3 vì có khí thoát ra, phương trình ion thu gọn:
2H+ + CO32- 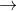 H2O + CO2
H2O + CO2
* Dùng dung dịch BaCl2 làm thuốc thử:
- Nhận ra dung dịch (NH4)2SO4 vì có kết tủa trắng, phương trình ion thu gọn:
Ba2+ + SO42- 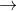 BaSO4
BaSO4
- Còn lại là dung dịch NH4Cl.
a.
(1) 3Cu + 8HNO3 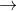 3Cu(NO3)2 + 2NO + 4H2O
3Cu(NO3)2 + 2NO + 4H2O
Hoặc: Cu + 4HNO3 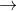 Cu(NO3)2 + 2NO2 + 2H2O
Cu(NO3)2 + 2NO2 + 2H2O
(2) 2Cu(NO3)2 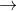 2CuO + 4NO2 + O2
2CuO + 4NO2 + O2
(3) 4NO2 + O2 + 2H2O 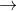 4HNO3
4HNO3
b.
* Dùng dung dịch HCl làm thuốc thử:
- Nhận ra dung dịch (NH4)2CO3 vì có khí thoát ra, phương trình ion thu gọn:
2H+ + CO32- 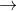 H2O + CO2
H2O + CO2
* Dùng dung dịch BaCl2 làm thuốc thử:
- Nhận ra dung dịch (NH4)2SO4 vì có kết tủa trắng, phương trình ion thu gọn:
Ba2+ + SO42- 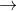 BaSO4
BaSO4
- Còn lại là dung dịch NH4Cl.
Câu hỏi liên quan
-

(3 điểm)
Cho các chất: anabazin; nicotin; nicotirin.
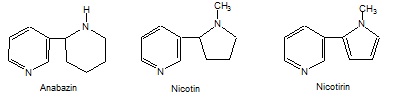
a) Viết phương trình phản ứng xảy ra khi cho mỗi chất trên tác dụng với HCl theo tỷ lệ mol 1 : 1.
b) Sắp xếp các chất theo chiều tăng dần tính bazơ.
c) Oxi hóa nicotin bằng K2Cr2O7 trong dung dịch H2SO4 thu được axit nicotinic. Viết công thức cấu tạo của axit nicotinic và so sánh nhiệt độ nóng chảy của nó với axit benzoic. Giải thích.
-

(1đ)
Cho Kb của CH3COO- ở 25oC là 5,56x10-10. Tính pH của dung dịch CH3COONa 0,5M ở 25oC.
-

(2 điểm)
1. Khi đốt cháy hoàn toàn 1 mol một ankan A thu được số mol CO2 nhỏ hơn 6, còn khi cho A tác dụng Cl2 theo tỉ lệ mol 1:1, có chiếu sáng, chỉ thu được một dẫn xuất monoclo duy nhất. Viết công thức cấu tạo thu gọn của A và các dẫn xuất monoclo tương ứng.
2. Khi trùng hợp buta-1,3-dien với xúc tác natri kim loại ngoài cao su buna còn có một loại polime có nhánh X và một sản phẩm phụ Y.
Viết phương trình phản ứng tạo thành X; Y. Biết rằng khi hidro hóa Y ta thu được etylxiclohexan
-

( 2 điểm):
Viết công thức cấu tạo của các hợp chất dị vòng sau đây:
a) 2-Metyl-5-phenylthiophen.
b) Axit 3-etylpirol-2-cacboxylic.
c) 2,6-Đi-tert-butylpiriđin.
d) Etyl piriđin-3-cacboxylat.
-

(3 điểm)
1. X là một hiđrocacbon. Hiđro hóa hoàn toàn X thì thu đuợc 3-etylhexan. Tỉ khối hơi của X so với Hiđro bằng 52. Nếu cho 10,4 gam X tác dụng hoàn toàn với lượng dư dung dịch bạc nitrat trong amoniac thì tạo được 31,8 gam một chất rắn có màu vàng nhạt. Lập công thức phân tử và viết các công thức cấu tạo có thể có của X.
2. Y là hỗn hợp gồm hidrocacbon CxHy (A) và H2. Sau khi đun nóng hỗn hợp Y với xúc tác Ni ta chỉ thu được một khí K duy nhất. Ở cùng điều kiện nhiệt độ và áp suất, tỷ khối của K so với H2 gấp ba lần tỷ khối hơi của Y so với H2. Mặt khác nếu đốt cháy hoàn toàn một lượng khác của K thu được 22 gam CO2 và 13,5 gam nước. Xác định công thức phân tử của A.
-

(1,5đ).
Viết các phương trình hoá học (ghi rõ điều kiện – nếu có) để hoàn thành sơ đồ phản ứng sau:
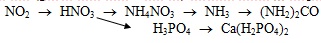
-

(3 điểm): a. Hoàn thành sơ đồ sau bằng các phương trình phản ứng:
N2
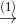 NH3
NH3 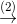 NO
NO 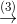 NO2
NO2b. Phân biệt 3 dung dịch riêng biệt sau bằng phương pháp hoá học:
K2CO3,KCl, K2SO4
-

(1đ)
Cho Ka của CH3COOH ở 25oC là 1,8x10-5. Tính pH của dung dịch CH3COOH 0,5M ở 25oC.
-

(3 điểm):
a. Cho 16 gam Fe2O3 tác dụng vừa đủ với V ml dung dịch HNO3 1,5M, thu được dung dịch chứa a gam muối. Viết phương trình phản ứng xảy ra, tìm các giá trị V và a.
b. Hòa tan hoàn toàn 4,86 gam kim loại Al vào dung dịch HNO3 loãng, dư, thấy thoát ra 2,24 lít khí NO (ở đktc và là khí thoát ra duy nhất), tính khối lượng muối tan có trong dung dịch sau phản ứng.
-

(1đ).
Viết công thức cấu tạo đầy đủ và công thức cấu tạo thu gọn, thu gọn nhất của các chất: etilen (C2H4); etanol (C2H5OH).
