Cho 6,175 gam Zn tác dụng vừa đủ với dung dịch chứa a mol HNO3. Sau phản ứng thu được dung dịch X và 0,448 lit hỗn hợp khí Y gồm NO, N2O. Tỉ khối hơi của Y so với H2 là 18,5. Cô cạn dung dịch X thu được b gam muối. Giá trị của a và b lần lượt là

Câu hỏi
Nhận biếtCho 6,175 gam Zn tác dụng vừa đủ với dung dịch chứa a mol HNO3. Sau phản ứng thu được dung dịch X và 0,448 lit hỗn hợp khí Y gồm NO, N2O. Tỉ khối hơi của Y so với H2 là 18,5. Cô cạn dung dịch X thu được b gam muối. Giá trị của a và b lần lượt là
Đáp án đúng: C
Lời giải của Luyện Tập 365
Gọi số mol của NO và NO2 lần lượt là x, y. Theo bài ta có:
x + y = 0,02; 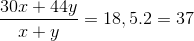
=> Số mol NO = n N2O= 0.01mol
Zn - 2e ---> Zn 2+ N+5 + 3e ---> N+2(NO)
0,095 0,19 0,01 0,03
2N +5 + 8e ---> N+1(N2O) 0,01 0,08
Áp dụng định luật bảo toàn e nhận thấy 0,19 # 0,11 => tạo cả NH4NO3
nZn x2 = nNOx3 + nN2Ox8 + nNH4NO3x8
=> số mol NH4NO3=0,01 => nHNO3=nNOx4 + nN2Ox10 + nNH4NO3x10 = 0,24 mol
m (NH4NO3 + Zn(NO3)2) = 0,01.80 + 0,095.189 = 18,755g
Gọi số mol của NO và NO2 lần lượt là x, y. Theo bài ta có:
x + y = 0,02; 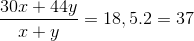
=> Số mol NO = n N2O= 0.01mol
Zn - 2e ---> Zn 2+ N+5 + 3e ---> N+2(NO)
0,095 0,19 0,01 0,03
2N +5 + 8e ---> N+1(N2O) 0,01 0,08
Áp dụng định luật bảo toàn e nhận thấy 0,19 # 0,11 => tạo cả NH4NO3
nZn x2 = nNOx3 + nN2Ox8 + nNH4NO3x8
=> số mol NH4NO3=0,01 => nHNO3=nNOx4 + nN2Ox10 + nNH4NO3x10 = 0,24 mol
m (NH4NO3 + Zn(NO3)2) = 0,01.80 + 0,095.189 = 18,755g
Câu hỏi liên quan
-

Nhận định nào dưới đây là đúng?
-

Trong công nghiệp, amoniac được điều chế từ nitơ và hiđrô bằng phương pháp tổng hợp: N2 (k) + 3H2 (k) <=> 2NH3 (k). Phản ứng theo chiều thuận là phản ứng tỏa nhiệt. Về lý thuyết, cân bằng trên sẽ dịch chuyển về phía tạo thành amoniac nếu
-

Trong các chất HF, HCl, HBr và HI thì
-

Có hai hi đrocacbon A, B đều là chất khí ở điều kiện thường, không phải là đồng phân của nhau.Khi đốt cháy hoàn toàn, mỗi chất đều tạo ra số mol nước gấp 3 lần số mol mỗi chất đã cháy. A và B thỏa mãn sơ đồ chuyển hóa sau: A
![\xrightarrow[600^{0}C]{Fe}](https://luyentap365.com/wp-content/picture/learning/exam/2013/1101/164_230_1.gif) X → Y → B → Cao su buna. Trong đó X, Y có cùng số lượng nguyên tử cacbon trong phân tử. Vậy Y là
X → Y → B → Cao su buna. Trong đó X, Y có cùng số lượng nguyên tử cacbon trong phân tử. Vậy Y là -

Đốt cháy hoàn toàn 0,1 mol este X thu được 0,3 mol khí CO2 và 0,3 mol H2O. Nếu cho 0,1 mol X tác dụng hết với NaOH thì thu được 8,2 gam muối. X là
-

Este X (MX =103 đvC) được điều chế từ một ancol đơn chức ( có tỉ khối hơi so với oxi lớn hơn 1) và một amino axit. Cho 25,75 gam X phản ứng hết với 300ml dung dich NaOH 1M, thu được dung dịch Y. Cô cạn Y thu được m gam chất rắn. Giá trị m là
-

Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai ancol đơn chức, cùng dãy đồng đẳng, thu được 15,68 lít CO2 (đktc) và 17,1 gam nước. Mặt khác, thực hiện phản ứng este hóa m gam X với 15,6 gam axit axetic, thu được a gam este. Biết hiệu suất phản ứng este hóa của hai ancol đều bằng 60%. Giá trị của a là
-

Cho các chất sau C6H5-NH2 (X); Cl-C6H4 -NH2 (Y); O2N-C6H4 -NH2 (Z); CH3-C6H4-NH2 (T). Chất có tính bazơ mạnh nhất là:
-

Đun nóng xenlulozơ với hỗn hợp HNO3 và H2SO4 đặc, thu được chất dễ cháy, nổ mạnh không có khói nên được dùng làm thuốc súng không khói. Sản phẩm đó là
-

Chia m gam hỗn hợp gồm Na2O và Al2O3 thành 2 phần đều nhau: - Phần 1: Hòa tan trong nước dư thu được 1,02 gam chất rắn không tan - Phần 2: Hòa tan hết trong dung dịch HCl 1M thì cần vừa đủ 140ml dung dịch HCl. Khối lượng hỗn hợp ban đầu m có giá trị bằng
