Nung 18,8 gam muối Cu(NO3)2 một thời gian, thu được 12,32 gam hỗn hợp rắn X. Hiệu suất phản ứng nhiệt phân là

Câu hỏi
Nhận biếtNung 18,8 gam muối Cu(NO3)2 một thời gian, thu được 12,32 gam hỗn hợp rắn X. Hiệu suất phản ứng nhiệt phân là
Đáp án đúng: B
Phương pháp giải
Khối lượng chất rắn giảm là khối lượng của khí thoát ra ⟹ mchất rắn giảm = mNO2 + mO2
Tính toán theo PTHH: Cu(NO3)2 → CuO + 2NO2↑ + 0,5 O2↑
Khối lượng chất rắn giảm là khối lượng của khí thoát ra ⟹ mchất rắn giảm = mNO2 + mO2
Tính toán theo PTHH: Cu(NO3)2 → CuO + 2NO2↑ + 0,5 O2↑
Lời giải của Luyện Tập 365
nCu(NO3)2 bđ = 0,1 mol
Đặt nCu(NO3)2 nhiệt phân = x mol
PTHH: Cu(NO3)2 → CuO + 2NO2↑ + 0,5 O2↑
x → x → 2x → 0,5x (mol)
Ta thấy khối lượng chất rắn giảm là khối lượng của khí thoát ra
⟹ mchất rắn giảm = mNO2 + mO2 ⟹ 46.2x + 32.0,5x = 18,8 - 12,32 ⟹ x = 0,06 mol
⟹ Hiệu suất quá trình nhiệt phân là: H% = 0,06/0,1 = 0,6 = 60%.
nCu(NO3)2 bđ = 0,1 mol
Đặt nCu(NO3)2 nhiệt phân = x mol
PTHH: Cu(NO3)2 → CuO + 2NO2↑ + 0,5 O2↑
x → x → 2x → 0,5x (mol)
Ta thấy khối lượng chất rắn giảm là khối lượng của khí thoát ra
⟹ mchất rắn giảm = mNO2 + mO2 ⟹ 46.2x + 32.0,5x = 18,8 - 12,32 ⟹ x = 0,06 mol
⟹ Hiệu suất quá trình nhiệt phân là: H% = 0,06/0,1 = 0,6 = 60%.
Câu hỏi liên quan
-

(3 điểm): a. Hoàn thành sơ đồ sau bằng các phương trình phản ứng:
Cu
 Cu(NO3)2
Cu(NO3)2  NO2
NO2  HNO3
HNO3b. Phân biệt 3 dung dịch riêng biệt sau bằng phương pháp hoá học:
(NH4)2CO3, NH4Cl, (NH4)2SO4
-

(3 điểm):
a. Cho 16 gam Fe2O3 tác dụng vừa đủ với V ml dung dịch HNO3 1,5M, thu được dung dịch chứa a gam muối. Viết phương trình phản ứng xảy ra, tìm các giá trị V và a.
b. Hòa tan hoàn toàn 4,86 gam kim loại Al vào dung dịch HNO3 loãng, dư, thấy thoát ra 2,24 lít khí NO (ở đktc và là khí thoát ra duy nhất), tính khối lượng muối tan có trong dung dịch sau phản ứng.
-

(1đ)
Nhiệt phân hoàn toàn hỗn hợp X gồm KNO3 và Cu(NO3)2 thu được hỗn hợp khí Y có tỉ khối so với oxi là d.
Tìm khoảng giá trị của d. Khi d = 1,3 thì % khối lượng của KNO3 trong hỗn hợp X là bao nhiêu?
-

( 2 điểm):
Viết các phương trình phản ứng thực hiện sơ đồ sau:
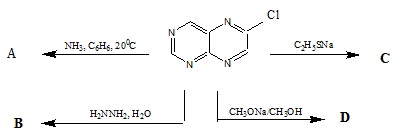
-

(1,5đ)
Viết các phương trình hoá học (ghi rõ điều kiện – nếu có) để hoàn thành sơ đồ phản ứng sau:
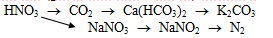
-

(1,5đ)
Cho dung dịch HNO3 loãng lần lượt tác dụng với: Al(OH)3; kim loại Zn (N2O là sản phẩm khử duy nhất).
Viết các phương trình hoá học dưới dạng phân tử và ion thu gọn. Nêu vai trò của HNO3 trong mỗi phản ứng.
-

(1đ)
Cho Ka của CH3COOH ở 25oC là 1,8x10-5. Tính pH của dung dịch CH3COOH 0,5M ở 25oC.
-

(4 điểm): Hoàn thành phương trình phân tử, viết phương trình ion thu gọn:
a. NaOH + HNO3
b. AgNO3 + NaCl
c. MgO + H2SO4
d. (NH4)2CO3 + HCl
-

(2 điểm)
1. Xác định các chất A, B, D, E và viết các phương trình phản ứng thực hiện sơ đồ sau:

Biết rằng khi đốt cháy 0,1 mol E thu được 0,9 mol CO2
2. Một sơ đồ để điều chế cao su Buna như sau, xác định M và viết các phương trình phản ứng:
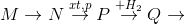 Cao su Buna
Cao su Buna -

(1đ)
Nhiệt phân hoàn toàn hỗn hợp X gồm KNO3 và Cu(NO3)2 thu được hỗn hợp khí Y có tỉ khối so với oxi là 1,25. Tính % khối lượng của KNO3 trong hỗn hợp X?
