Cấu hình electron của nguyên tố Fe (Z = 26) là

Câu hỏi
Nhận biếtCấu hình electron của nguyên tố Fe (Z = 26) là
Đáp án đúng: A
Phương pháp giải
- Quy ước cách viết cấu hình electron nguyên tử:
+ Số thứ tự lớp electron bằng các chữ số: 1, 2, 3
+ Phân lớp được kí hiệu bằng chữ cái thường: s, p, d, f
+ Số electron trong phân lớp được ghi bằng chỉ số ở phía trên bên phải kí hiệu của phân lớp: s2, p6, d10…
- Cách viết cấu hình electron nguyên tử:
+ Xác định số electron của nguyên tử.
+ Các electron được phân bố theo thứ tự tăng dần các mức năng lượng AO, tuân theo các nguyên lí Pau-li, nguyên lí vững bền và quy tắc Hun.
+ Viết cấu hình electron theo thứ tự các phân lớp trong 1 lớp và theo thứ tự của các lớp electron.
+ Lưu ý: các electron được phân bố vào các AO theo phân mức năng lượng tăng dần và có sự chèn mức năng lượng. Tuy nhiên, khi viết cấu hình electron, các phân mức năng lượng cần được sắp xếp lại theo từng lớp.
- Quy ước cách viết cấu hình electron nguyên tử:
+ Số thứ tự lớp electron bằng các chữ số: 1, 2, 3
+ Phân lớp được kí hiệu bằng chữ cái thường: s, p, d, f
+ Số electron trong phân lớp được ghi bằng chỉ số ở phía trên bên phải kí hiệu của phân lớp: s2, p6, d10…
- Cách viết cấu hình electron nguyên tử:
+ Xác định số electron của nguyên tử.
+ Các electron được phân bố theo thứ tự tăng dần các mức năng lượng AO, tuân theo các nguyên lí Pau-li, nguyên lí vững bền và quy tắc Hun.
+ Viết cấu hình electron theo thứ tự các phân lớp trong 1 lớp và theo thứ tự của các lớp electron.
+ Lưu ý: các electron được phân bố vào các AO theo phân mức năng lượng tăng dần và có sự chèn mức năng lượng. Tuy nhiên, khi viết cấu hình electron, các phân mức năng lượng cần được sắp xếp lại theo từng lớp.
Lời giải của Luyện Tập 365
Cấu hình electron của nguyên tố Fe (Z = 26) là 1s22s22p63s23p63d64s2.
Cấu hình electron của nguyên tố Fe (Z = 26) là 1s22s22p63s23p63d64s2.
Câu hỏi liên quan
-

R là nguyên tố nhóm A, công thức hợp chất khí của R với hiđro là RH3. Trong hợp chất oxit cao nhất của R, oxi chiếm 56,34% về khối lượng.
a.Xác định tên của R.
b.Viết công thức electron, công thức cấu tạo phân tử hợp chất của R với hiđro.
-

Nguyên tử X ở trạng thái cơ bản có 3 lớp electron và có 1 electron độc thân.
a) Viết cấu hình electron của X và xác định vị trí của X trong bảng tuần hoàn.
b) X là nguyên tố s, p, d hay f? X là kim loại hay phi kim?
c) Viết công thức oxit cao nhất và công thức hiđroxit tương ứng. Oxit và hiđroxit tương ứng là axit hay bazơ? Viết phản ứng của chúng với dung dịch NaOH (nếu có).
-

Trong phản ứng 3NO2 + H2O → 2HNO3 + NO. NO2 đóng vai trò gì?
-

Ion X- có cấu hình electron là 1s22s22p6. Trong ion X- số hạt mang điện nhiều hơn số hạt không mang điện là 9. Viết kí hiệu nguyên tử của nguyên tố X.
-

Trong tự nhiên Clo có hai đồng vị bền: 3717Clchiếm 25% tổng số nguyên tử, còn lại là 3517Cl. Tính thành phần % theo khối lượng của 3717Cl trong HClO3 ? ( lấy H=1, O= 16)
-

Số e độc thân của nguyên tử lưu huỳnh (Z=16) bằng:
-

Phương trình hoá học nào sau đây là phản ứng oxi hóa khử?
-

Cho cân bằng sau trong bình kín: 2NO2 (k)
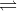 N2O4 (k) ở 250C
N2O4 (k) ở 250C (màu nâu đỏ) (không màu)
a) Viết công thức electron, công thức cấu tạo của NO2 và N2O4. Xác định cộng hoá trị và
số oxi hoá của N trong các hợp chất đó. Tại sao NO2 có thể đime hoá thành N2O4.
Cho N (Z=7); O(Z=8)
b) Khi giảm nhiệt độ thì tỉ khối của hỗn hợp khí so với H2 tăng lên. Vậy khi hạ nhiệt
độ của bình thì màu nâu đỏ đậm lên hay nhạt đi? Phản ứng thuận toả nhiệt hay thu
nhiệt? Tại sao?
c) Khi tăng áp suất thì cân bằng trên chuyển dịch theo chiều nào? Tại sao?
d) Cho 18,4 gam N2O4 vào bình dung tích 5,904 lít ở 270C. Lúc cân bằng, áp suất của
hỗn hợp khí trong bình là 1 atm (nhiệt độ 270C).
-

Sự oxi hóa là:
-

Cân bằng các phản ứng oxi hóa- khử sau bằng phương pháp thăng bằng electron và cho biết chất oxi hóa, chất khử, sự oxi hóa, sự khử ở mỗi phản ứng:
a.Mg + H2SO4 → MgSO4 + S + H2O
b.NH3 + CuO → Cu + N2 + H2O
